老化を遅らせることは可能か?小さな蜂に秘められた能力を検証
老化の研究において、近年注目を集めているのが「生物学的年齢」という概念です。
カレンダー上の年齢(暦年齢)とは異なり、生物学的年齢は体内の分子や細胞の状態をもとに算出される「実際の老化度合い」を示すものです。
近年ではDNAメチル化の変化を測定することでこのバイオエイジを推定する「エピジェネティック・クロック(分子老化時計)」が発展しています。
ところが、多くの昆虫はDNAメチル化をほとんど持たず、こうした分析が困難でした。

そんな中で登場したのがキョウソヤドリコバチ(学名:Nasonia vitripennis)です。
このハチは、体長2〜2.5mmほどの小さな寄生蜂で、ハエの蛹に卵を産みつけ、幼虫が体内から宿主を食べるという生態を持っています。
小さくても研究者にとっては極めて有用な生物です。
というのも、キョウソヤドリコバチは、哺乳類と同様のDNAメチル化システムを備えた数少ない昆虫だからです。
しかも寿命が非常に短く(約1か月)、エピジェネティックな老化を研究するモデル生物として理想的な条件を満たしています。
さらにこのハチの幼虫は、一定の環境条件(低温・短日)にさらされることで「diapause」と呼ばれる発育停止状態(いわば昆虫の冬眠)に入ることが知られていました。
研究チームはこの休眠に着目し、「この一時停止状態が、その後の老化速度に影響を与えるのではないか?」という仮説を立てました。

そこで彼らは、以下のような実験を行いました。
キョウソヤドリコバチの母親を、低温かつ短い光周期(20℃、明8時間/暗16時間)で飼育しました。
その結果、生まれた幼虫が自発的に休眠に突入。
休眠中は4℃かつ完全な暗闇で3か月間保存されました。
その後、通常環境(25℃、光12時間/暗12時間)に戻して、成虫へと成長させました。
対照群として、休眠を経ない通常育成の個体も飼育。
これら2群の成虫について、老化速度や寿命、DNAメチル化の状態を比較しました。
幼虫期に休眠したハチは老化が遅くなり寿命が36%伸びる
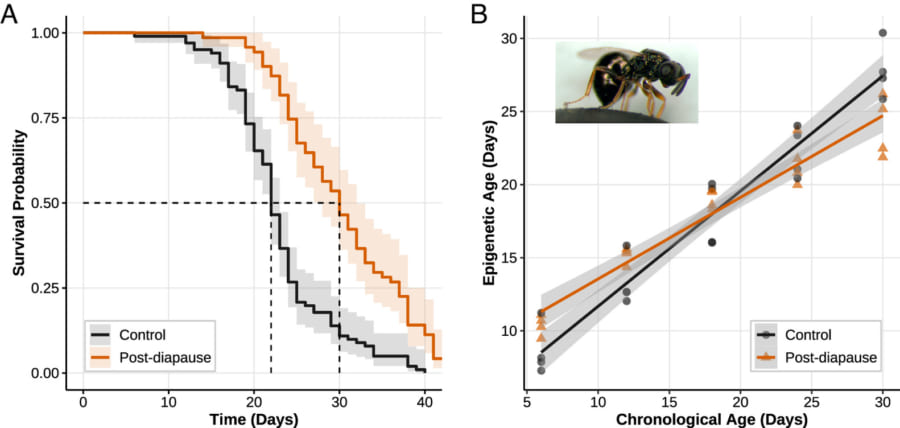
実験の結果、休眠を経験した個体は、寿命が平均で36%も長くなっていました。
対照群の成虫が平均22日で死ぬのに対し、ディアポーズ群は平均30日も生きたのです。
また、DNAメチル化を用いて構築されたエピジェネティック・クロックによる分析では、老化速度が、休眠を経験しなかった個体と比較して、成虫化後に約29%も遅く進行することが判明しました。
つまり、分子レベルでも「若い状態」が長く保たれていたのです。
さらに興味深いのは、目覚めた直後(成虫化6日目)に休眠群のほうがむしろ生物学的年齢が高く出る(分子年齢が2.8日ほど高い)にもかかわらず、その後の老化進行が非常に遅く、最終的には対照群よりも分子年齢が若い状態になっていたという点です。
この現象は、休眠中にもわずかな老化は進んでいたものの、その期間に老化のスピードを再設定するような分子レベルのリプログラミング(再構成)が起こったことを示唆しています。
そして研究チームは、老化速度の変化が哺乳類にも共通する代謝系と関連していることを発見しました。
つまり、この小さなハチの老化抑制メカニズムは、人間の生物学的老化にも応用できる可能性があるのです。

もちろん、今回の研究は基礎生物学的な段階であり、すぐに人間に応用できるわけではありません。
しかし、老化という普遍的な課題に対し、自然界のメカニズムからヒントを得られることを示した意義は大きいといえます。
研究者らは今後、「DNAメチル化領域の編集による老化制御」「哺乳類でも同様の生物学的年齢の再構成が可能かを調べる研究」「人間の出生前・乳幼児期の環境が老化に与える影響の解明といった応用研究」を計画しています。
この研究は、「老化は止められない」というこれまでの思い込みを根本から覆すものです。
わずか数ミリの昆虫が、私たち人類の「老化の針をゆっくり動かす」ための大きなヒントを与えてくれました。

































![よーく聞いてね!3つのヒントで学ぶ!どうぶつカード ([バラエティ])](https://m.media-amazon.com/images/I/51zT3OcliFL._SL500_.jpg)
![マモルーム お部屋まるごと予防空間 ダニ用 [2ヵ月用セット] ダニアレル物質の生成抑制・ダニを除去しやすくなる ダニよけ 加熱蒸散機 ダニ対策 (アース製薬)](https://m.media-amazon.com/images/I/413VgtLwPgL._SL500_.jpg)



























