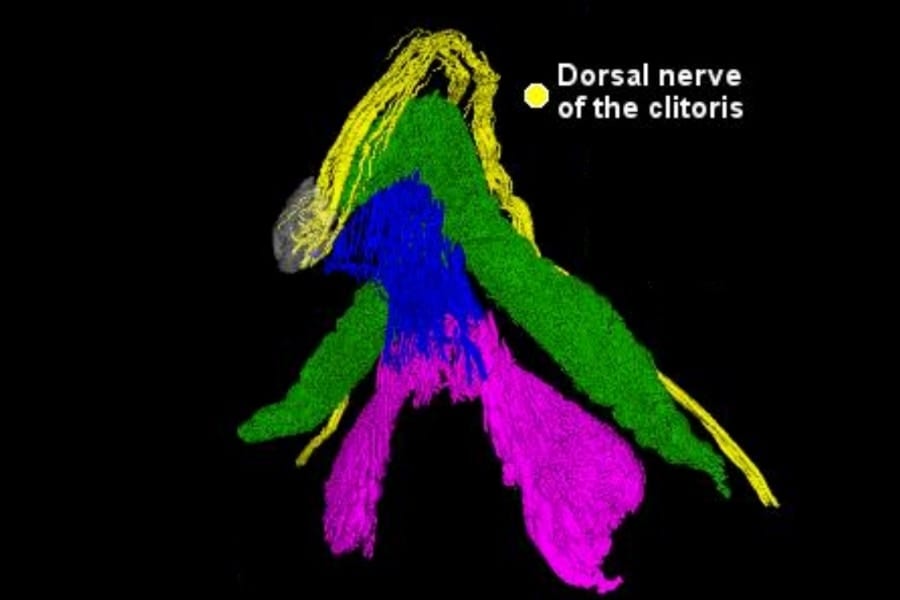
【研究背景】安全神話の裏でくすぶる『なぜ効くか』問題

今回は鎮痛の仕組みを扱うことから、非常に多くの物質名や複雑な細胞の仕組みが出てきます。
そこでまずは、生物学や薬学が苦手な人向けに、ざっくり解説した版を作成することにしました。
ざっくり解説版を読むだけで大方の把握はできますが、さらに詳しい解説が欲しい人は続く本解説に進んでください。
研究の背景の「ざっくり解説版」
アセトアミノフェンは、19世紀末に誕生して以来、世界中で「当たり前の痛み止め」として使われてきました。
ところが、その仕組みは驚くほど謎に包まれていたのです。
これまでは、「脳内で作られる“快楽物質”や“麻薬のような物質”を増やして痛みを和らげる」という説が有力でした。
しかし最近、「アセトアミノフェンは脳内の“別バージョンの鎮痛物質”をわざと減らすことで痛みを抑えているかもしれない」という新しい考えが注目を集めています。
問題の“別バージョンの鎮痛物質”とは、2-AGと呼ばれる成分です。
鎮痛物質を減らして痛みが減るというと奇妙に聞こえるかもしれませんが、実は脳にはさまざまな回路があり、ある回路では2-AGが増えると逆に痛みが強まる可能性があるのです。
これは脳の仕組みが“単純に快楽物質を増やせば痛みは減る”とは限らない、ということを示唆しています。
たとえば、ある回路では2-AGが「痛みをやわらげるブレーキ」をさらにブレーキするような働きをしてしまい、結果として痛み信号が増幅される、という二重のしくみが起こり得るのです。
そこでアセトアミノフェンは、2-AGを作る“工場”を抑えてその量を減らすことで、こうした逆効果の回路を静かにさせている可能性があります。
つまり、「必要以上に働きすぎるブレーキをブロックすることで、痛みの伝わりすぎを防ぐ」というイメージです。
この点が、従来説の「快楽物質を増やして“受け取り手”を刺激する」とは真逆の発想で、学界からも初めは懐疑的な声が上がったといいます。
そこで今回は別バージョンの鎮痛物質「2-AG」を減らすことが本当にアセトアミノフェンの鎮痛の仕組みかを確かめることにしました。
研究背景の本解説
アセトアミノフェンは19世紀末に初めて合成され、1950年代からタイレノールの名で世界中に広まり、現在では最も一般的な鎮痛・解熱薬の一つとして知られています。
比較的安全とされ市販薬にも多用されている一方、過剰摂取による肝障害が原因で毎年アメリカで約500人もの死亡者を出し、世界的にも急性肝不全の主要な要因となっています。
それほど多くの人が日常的に使っているにもかかわらず、その正確な鎮痛メカニズムは「いまだによく分かっていない」とされてきました。
従来提案されてきた仮説としては、中枢でのシクロオキシゲナーゼ(COX)阻害やセロトニン経路の関与などが挙げられますが、とりわけ「エンドカンナビノイド系が関わっているのではないか」という説が注目されてきました。
エンドカンナビノイドとは、体内で作られる内因性のカンナビス様物質の総称で、CB1受容体に結合して痛みを抑制すると考えられています。
実際、アセトアミノフェンがカンナビノイド受容体を欠損したマウスでは鎮痛効果を示さないとの実験結果もあり、「アセトアミノフェンはエンドカンナビノイド量を増やし、CB1受容体を活性化することで鎮痛をもたらす」という説が有力でした。
特に、アセトアミノフェンから生成される代謝物AM404がエンドカンナビノイドであるアナンダミドを脳内で増やすことで鎮痛が起こるという仮説は広く支持されてきました。
しかしこの仮説には、AM404が脳内で十分量生成されるかどうかなど、不確かな点も多く指摘されています。
さらにアナンダミドを分解するFAAH(脂肪酸アミドヒドロラーゼ)を欠損させたマウスでもアセトアミノフェンの鎮痛効果が部分的に見られるケースがあり、これだけでは説明しきれない仕組みがある可能性が高まっていました。
そこでインディアナ大学の研究チーム(ミカエラ・ドボラコバ博士ら)は、アセトアミノフェンともう一つの主要エンドカンナビノイド2-AGの関係に注目し、その作用機序を根本から再検討する研究を実施しました。
2-AGは脳内で非常に豊富に存在し、CB1受容体を活性化する役割を担う一方、これを合成する酵素DAGLαが欠損したマウスでは痛みの感受性が低い(鎮痛状態にある)という報告もありました。
もし「エンドカンナビノイドを増やす」のではなく「2-AGを減らす」ことで痛みを抑える回路が存在するなら、アセトアミノフェンの謎を解き明かすカギになるかもしれない――研究チームはその仮説を実験的に検証したのです。
























![クリーンプラネット [つけ置き強力洗剤] デトックス丸洗浄 プロフェッショナル 300g (衣類用漂白剤・非塩素タイプ)](https://m.media-amazon.com/images/I/51WGutdz9PL._SL500_.jpg)




![マイクロSDカード 512GB 高互換性 micro sdカード microSDXC メモリーカード 大容量 ミニSDカード 高速データ転送 TFカード SD変換アダプター付属 [並行輸入品]](https://m.media-amazon.com/images/I/516JSQaVLJL._SL500_.jpg)