自己組立「人工ウイルス粒子」の製造— 細胞が自ら免疫を刺激

「いいとこ取り」を実現するために、研究チームはまずワクチンの設計からスタートしました。
まずチームが考えたのは、「どうすれば免疫が本物のウイルスが来た!と勘違いしてくれるような粒子が作れるのか?」ということでした。
そこで彼らが注目したのが、ウイルスに似た「ナノ粒子」です。
ナノ粒子というのは、「ナノメートル」というごく小さな単位(髪の毛の太さの数万分の一)の粒子を指します。
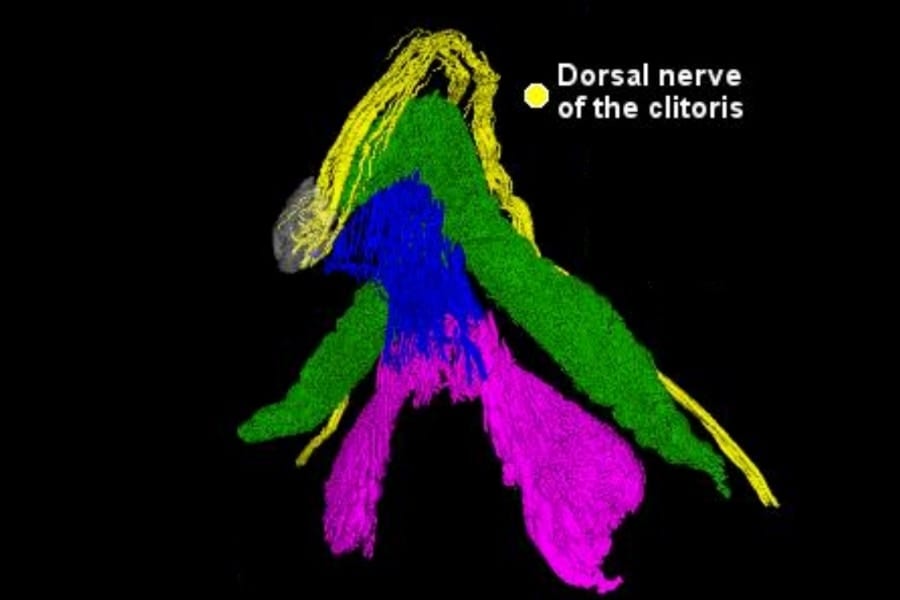
今回作った粒子は、60個の部品(サブユニット)が自動的に集まって、数十ナノメートル級の直径をもつ球状の粒子を作るように設計されています。
これはちょうど、サッカーボールのように多数のパネルが組み合わって自動でボールの形になる仕組みと似ています。
そして重要なのは、この粒子の表面に新型コロナウイルス特有の「スパイクタンパク質」の一部(RBDという部分)が約60個、突き出るようにしたことです。
これは例えるなら、ウイルスが細胞に侵入するときに使う「鍵」を60個も粒子表面にずらりと並べているような状態です。
ここで疑問が湧くかもしれません。
「そんなに多くの鍵を並べる必要があるの?」と。
実はこの仕掛けがとても大切です。
免疫細胞は敵を記憶するとき、ただ敵の部品を見るだけではなく、敵がどのように並んでいるか、その「見せ方」に非常に敏感なのです。
同じ鍵(タンパク質)が規則的に並んでいると、それをより強力で重要な敵として認識します。
このため、たくさんの鍵を一気に並べて見せることで、免疫を強烈に刺激できるというわけです。
しかし、問題はこれを実際にどう作り出すかです。
そこで研究者たちは、「mRNAワクチン」の仕組みを利用しました。
mRNAというのは、タンパク質を作るための「設計図」だという話を先にも触れましたね。
研究者たちはこの粒子の60個の部品それぞれを作るための情報を、このmRNAの形で細胞に届けることを考えたのです。
この設計図が細胞に取り込まれ、部品が作られれば、あとは自動でウイルスを模した粒子が組み立てられていきます。
さて、この新型ワクチンのアイデアは画期的で魅力的ですが、実際にそれがうまくいくのかどうかを確かめるために、研究チームはマウスを使った実験を行いました。
マウスに今回の新型ワクチンと、従来のタイプのmRNAワクチン(新型コロナのスパイク蛋白質だけを作るもの)をそれぞれ接種し、免疫の反応を比較しました。
その結果、まず確認されたのは「中和抗体」と呼ばれるウイルスを無力化する抗体の量でした。
ここで驚くべきことに、新型ワクチンを接種したマウスでは、中和抗体が従来のmRNAワクチンと比べて5〜28倍も高くなったのです。
さらに注目すべきは投与量です。
わずか0.2マイクログラムという少ない量の新型ワクチンでも、従来ワクチンの比較的多い量(5マイクログラム)を使った場合と同じくらいの抗体量が得られました。
25分の1の量で同等の反応が見られたことは、効率が大幅に改善される可能性を示しています。
この結果は、副反応(ワクチンの副作用)を減らせる可能性も意味しています。
ただし、今回の研究では安全性や副反応を調べる試験は行われていないため、この点は今後の検証が必要です。
さらに重要なこととして、この新しいワクチンでは、従来型のタンパク質粒子ワクチンでは難しい「キラーT細胞(CD8+ T細胞)」と呼ばれる細胞性免疫も強く誘導されました。
最後に研究者たちは、実際にウイルスをマウスに感染させ、ワクチンの効果を検証しました。
すると、新型ワクチンを接種したマウスの肺では、ウイルスがほとんど検出されないほど感染が抑えられていました。
さらに、免疫から逃れる能力が高いオミクロン株(BA.5)を感染させた場合でも、新型ワクチンを接種したマウスは体重の減少が抑えられ、肺に残るウイルス量も低いか、検出されないほどでした。
これは、今回のワクチンがSARS-CoV-2の異なる株に対しても効果を示す可能性があることを示唆しています。

























![クリーンプラネット [つけ置き強力洗剤] デトックス丸洗浄 プロフェッショナル 300g (衣類用漂白剤・非塩素タイプ)](https://m.media-amazon.com/images/I/51WGutdz9PL._SL500_.jpg)




![マイクロSDカード 512GB 高互換性 micro sdカード microSDXC メモリーカード 大容量 ミニSDカード 高速データ転送 TFカード SD変換アダプター付属 [並行輸入品]](https://m.media-amazon.com/images/I/516JSQaVLJL._SL500_.jpg)