AIの力でタンパク質の組み合わせを解明する

「AlphaFold」はDNAの情報をもとにタンパク質の立体構造を予測するために開発された人工知能です。
「AlphaFold」は2018年に開発されてから急速な進化を遂げており、2022年には既知のほぼ全てにあたる2億種類以上のタンパク質の構造の予測が完了したことが知られています。
タンパク質の構造予測には以前からAIが使われていましたが、「AlphaFold」は正確性や速度において比類ない成績を収めています。
またこの「AlphaFold」はタンパク質同士が細胞内部ででどのように組み合わさるかを予測する機能も備えていました。
そこで研究者たちが栄養センサーの組み合わせを「AlphaFold」に調べさせたところ、5量体として知られる美しい構造が出現しました。
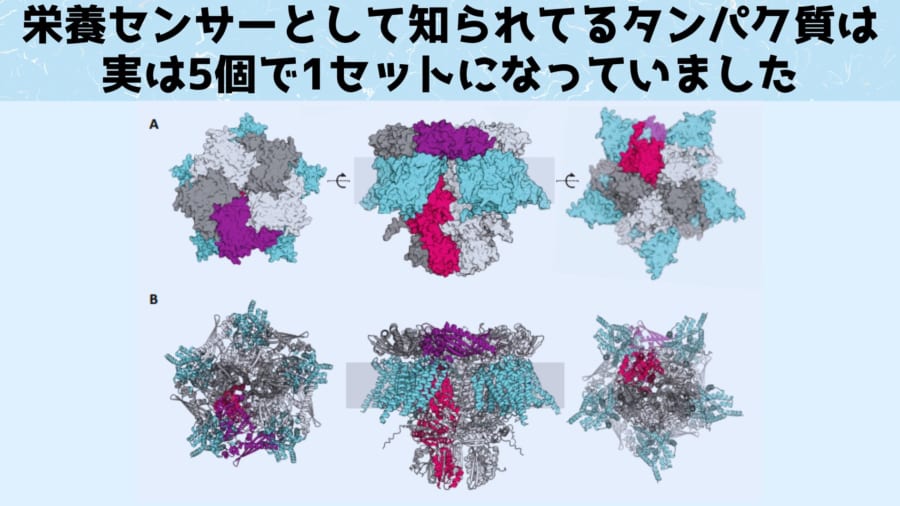
またこの5量体の構造を調べると、中央部分位はイオンを通過させられるトンネル状の通路が存在していることがわかりました。
この結果は、これまで単体で働くと思われていた栄養センサーが、実は5個で1セットとなるイオンチャンネルを構成している可能性を示します。
しかしAIによる予想が現実世界に当てはまるかを確かめるには、人間による実験が必要でした。
そこで研究者たちは細菌の遺伝子を操作し、常にトンネルが開きっぱなしになるような変異体を作りました。
するとこの変異体は周囲に栄養が全くない状態でも、内部からイオンを放出させて電気的な信号を発生させ、周囲のバリアを脱ぎ捨て生命活動を再開させることが判明します。
(※胞子化しているときの細菌は内部に復活時に信号となるような陽イオンが蓄えられていると考えられます)
逆に常に通路が閉まっているように操作した細菌ではイオンの放出が観察されず、栄養があっても胞子の覚醒は起きませんでした。
この結果は、細菌の目覚めが5個の栄養センサータンパク質からなる複合体の内部が「開いている」か「閉まっている」かで決まることを示します。
研究を指揮したラドナー氏は今回発見された仕組みについて「一度知ってしまえば(簡単に)納得できるものですが、事前に想像することは不可能でした」と述べています。
事実、細菌が復活するために使う栄養センサーの存在は50年以上前から知られていたにもかかわらず、それが5量体をしており、電気的な方法(イオンの流れ)で目覚めの信号を発していることが突き止められたのは、今回の研究がはじめてです。
また今回の研究は単に興味深いだけでなく、今後の人間の健康にとっても重要な意味を持つでしょう。
これまで人類はさまざまな方法を使って缶詰などの保存食の滅菌を行ってきましたが、胞子状態の細菌は滅菌に抵抗する可能性があり、食中毒の原因にもなります。
また人体に悪影響を及ぼす細菌のなかには、胞子化することで抗生物質をやり過ごすものも知られています。
ですが今回の研究によって胞子化を維持したり解除させる仕組みが明らかになりました。
この仕組みを上手く利用することができれば、細菌を胞子化させずに滅菌したり、全ての細菌を胞子化した状態に押しとどめて人体や食品への悪影響を封じることもできるでしょう。































![シルバーバック かわいい海の生きもの CUBE 2X2 キューブ ツーバイツー|海の生き物デザイン 立体パズル スピードキューブ 5cm 子ども〜大人向け 知育 ギフトに最適 ([バラエティ])](https://m.media-amazon.com/images/I/41EJOOLgGXL._SL500_.jpg)