脳オルガノイドがもたらす痛み研究の未来
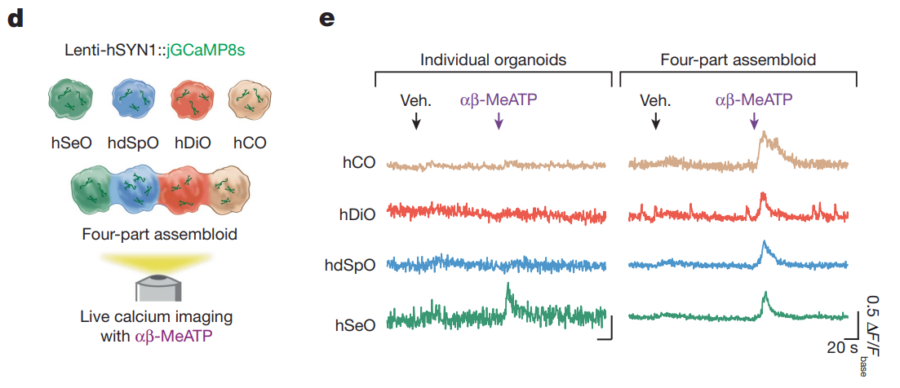
今回の成果が示す大きな意義は、試験管内でありながらヒトの痛覚回路を“ほぼ本物と同じ順序”で再現し、遺伝子変異や薬剤の影響をダイレクトに検証できるという点です。
これまで痛みの研究では、動物実験で得られた知見が人間の症状や反応とは異なる場合が少なくありませんでした。
ヒト由来の細胞で作られたオルガノイドを使えば、そうした種差の問題を大きく減らせるうえ、動物実験では扱いづらい先天性の痛覚異常や過敏症なども、比較的容易にモデル化できる可能性が広がります。
また、今回のモデルを用いることで、どの段階で痛みが“強化”あるいは“抑制”されるのか、どんな遺伝子異常が回路全体の働きを崩すのかを、リアルタイムで観察できるようになりました。
実際、SCN9Aの欠損が回路全体の同期活動を弱めることが判明したのは大きな発見であり、痛覚の治療標的を再考するヒントにもなりそうです。
逆に、痛みを過剰に増幅する変異型では、末端からのシグナルが過度に強まって脊髄や視床、大脳皮質まで連鎖的に“暴走”する様子が観察されました。
こうしたエビデンスは、慢性痛や難治性疼痛などの仕組み解明にも役立つかもしれません。
ただし、血管系や免疫細胞がほとんど含まれないオルガノイドであるがゆえに、まだ本物の体内環境とまったく同じとは言えません。
将来的には、栄養供給や炎症反応の研究もできるように改良が進む見込みです。 さらに成熟度を高めることで、より長期的な発達過程の再現や、末端の感覚受容器そのものを含む複合モデルなども期待されます。
もし皮膚オルガノイドや血管網と組み合わせることができれば、痛み刺激の発生から脳への伝達までを、より正確にトレースするシステムへと進化するかもしれません。
とはいえ、人間の痛覚を“ミニチュア回路”として観察できるようになったのは画期的です。
これは単なる基礎研究にとどまらず、慢性痛や先天性無痛症の治療薬開発の加速や、オーダーメイド医療の一助となることが期待されます。
今後、この技術がさらに発展し、オルガノイドを使って他の感覚(たとえば温度や触覚だけでなく視覚など)も含めた総合的な脳機能の解明が進めば、脳科学と医療の境界をまたいだ新しい扉が開かれるかもしれません。

























![マモルーム お部屋まるごと予防空間 ダニ用 [2ヵ月用セット] ダニアレル物質の生成抑制・ダニを除去しやすくなる ダニよけ 加熱蒸散機 ダニ対策 (アース製薬)](https://m.media-amazon.com/images/I/413VgtLwPgL._SL500_.jpg)


![よーく聞いてね!3つのヒントで学ぶ!どうぶつカード ([バラエティ])](https://m.media-amazon.com/images/I/51zT3OcliFL._SL500_.jpg)



























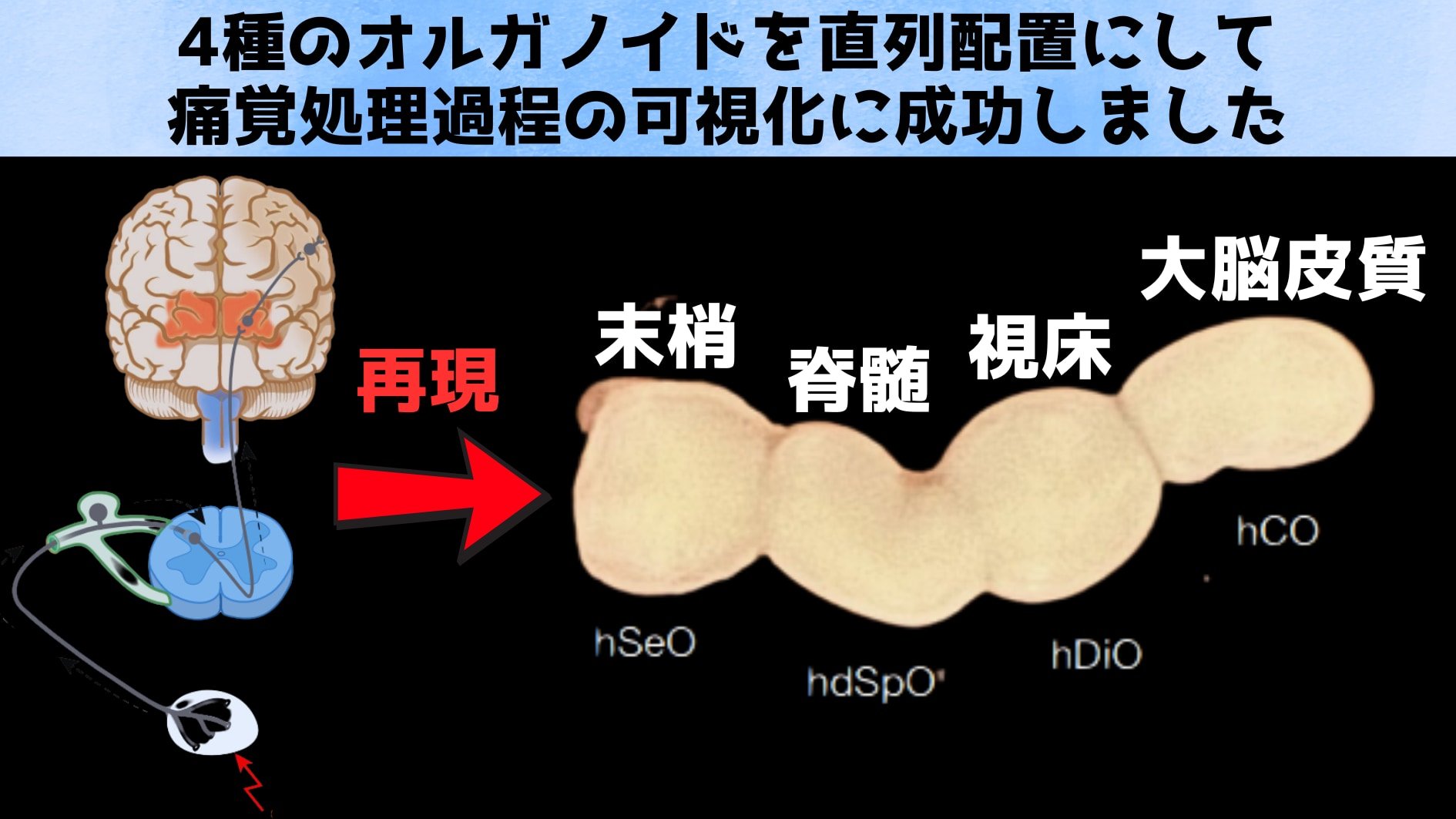
痛みのルートが分かれば薬ではなくて直接その信号だけを遮断して痛みを止める、麻酔に代わる鎮痛の手法とかも開発できそうでいいですね。